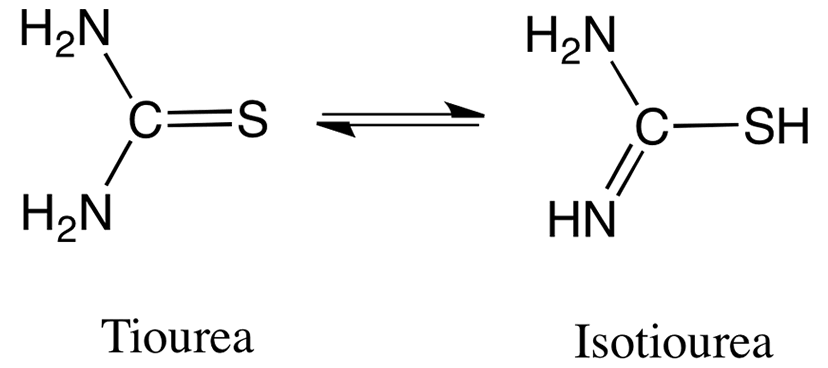
Tiourea es un compuesto orgánico organosulfurado. Es estructuralmente similar a la urea, excepto que el átomo de oxígeno se sustituye por un átomo de azufre, pero las propiedades de la urea y tiourea difieren significativamente. La tiourea es un compuesto químicamente interesante, que tiene tres grupos funcionales: amino, imino y tiol. Esto es resultado de la tautomería entre la tiourea y isotiourea.
Debido a esta polifuncionalidad y también debido a sus propiedades de formación de complejos, la tiourea ha sido ampliamente utilizada durante más de 40 años. Sus usos más importantes son como material de partida para heterociclos que contienen nitrógeno y azufre y el ácido formamidinsulfínico (dióxido de tiourea), también se utiliza como un socio de reacción para aldehídos, y como componente de compuestos de adición y complejos.
Los derivados de la tiourea son compuestos térmicamente estables, en su mayoría cristalinos. Pueden ser producidos con buenos rendimientos a partir de materiales de partida fácilmente disponibles por síntesis simples. Esta clase de compuestos, que se describe, han ganado importancia en el sector farmacéutico, en la fitosanidad, en diversas aplicaciones técnicas, y en la síntesis de heterociclos.
Propiedades Físicas de la Tiourea
La Tiourea, 2-tiourea, CH4N2S, es un sólido blanco, sin olor, y cristaliza en una estructura bipiramidal rómbica con cuatro moléculas por celda unidad. Es el único cristal molecular conocido que es ferroeléctrico dentro de un cierto rango de temperatura.
Grupo espacial D216h- Pnma.
La tiourea es soluble en disolventes polares próticos y apróticos (ver Tabla 1) e insoluble en los no polares.
Tabla 1. Solubilidad de tiourea
| En H2O | ||||||
|---|---|---|---|---|---|---|
| Temperatura,ºC | 0 | 20 | 40 | 60 | 80 | 100 |
| Solubilidad, g / 100 g | 4.9 | 13.7 | 30.7 | 70.9 | 138 | 233 |
| en MeOH | ||||||
|---|---|---|---|---|---|---|
| Temperatura, ◦C | 25 | 40.7 | 53.7 | 61.9 | ||
| Solubilidad, g / 100 g | 11.9 | 16.4 | 22 | 24.6 |
| en EtOH | ||||||
|---|---|---|---|---|---|---|
| Temperatura, ◦C | 20 | 31.9 | 45 | 58 | 64.7 | |
| Solubilidad, g / 100 g | 3.8 | 4.7 | 6.3 | 8.5 | 9.8 |
La tiourea no tiene ningún punto de fusión definido, ya que se re-organiza de manera relativamente rápida a rodanuro de amonio (NH4 SCN) a partir de los 135 ºC. Con un calentamiento rápido, se ha determinado un punto de fusión de 180 ºC. El calor de combustión a volumen constante es de 1482,2 kJ / mol (19,47 kJ / g), y a presión constante de 1485.6kJ / mol (19.52kJ / g).
Propiedades Químicas de la Tiourea
Aunque es conocida sólo en una forma, la tiourea también puede reaccionar como su tautoméro, el iminotiol. Sales tales como (NH2)2CS · HNO3 o (NH2)2CS · H2SO4 se forman con ácidos fuertes. Se pueden sintetizar compuestos de adición y complejos con óxidos metálicos o sales inorgánicas en solución ácida, por ejemplo, [Cr {(NH2) 2CS}3] Cl3.
En solución alcalina, un gran número de iones de metales pesados puede precipitar cuantitativamente como sulfuros con tiourea. Estos precipitados se filtran fácilmente, de modo que el método puede ser utilizado para la determinación analítica de sales metálicas. La producción de capas de PbS sensibles a la luz de y la purificación de las aguas residuales que contienen mercurio se basan en esta reacción.
La tiourea forma clatratos (compuestos de inclusión) con hidrocarburos alifáticos ramificada y cíclicos. Esta propiedad se puede utilizar, por ejemplo, para la separación de hidrocarburos alifáticos de cadena ramificada y de hidrocarburos de cadenas lineales.
La tiourea también se puede alquilar y acilar, y reacciona con aldehídos y cetonas. Con formaldehído, por ejemplo, se forma N- (hidroximetil) tiourea (H2 N-CS-NH-CH2-OH), que condensa en productos tipo resina con la calefacción. Por condensación de tiourea con clorocetonas, dicetonas, hidroxicetonas, ácidos oxocarboxílicos, y derivados cetónicos similares, pueden ser producidos un gran número de heterociclos. A partir de 2-halocetonas o 2-haloaldehídos (en forma enol) se forman derivados del 2-aminotiazol:
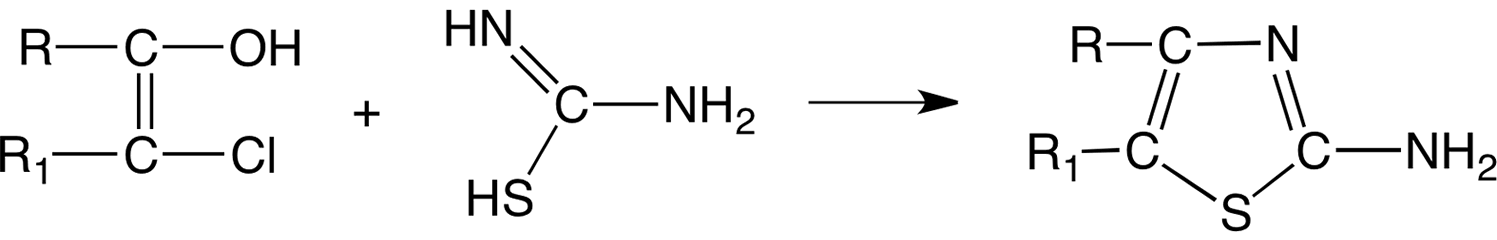
1,1-dihaloalcanos condensan con tiourea para 1,3,5-ditiazinas:
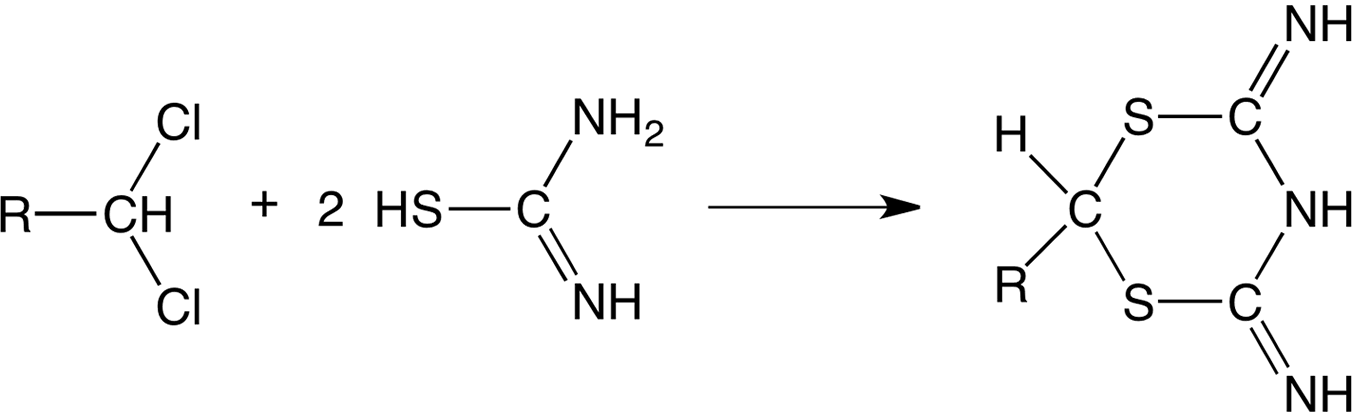
2-hidroxicetonas dan 4-imidazolina-2- tionas:
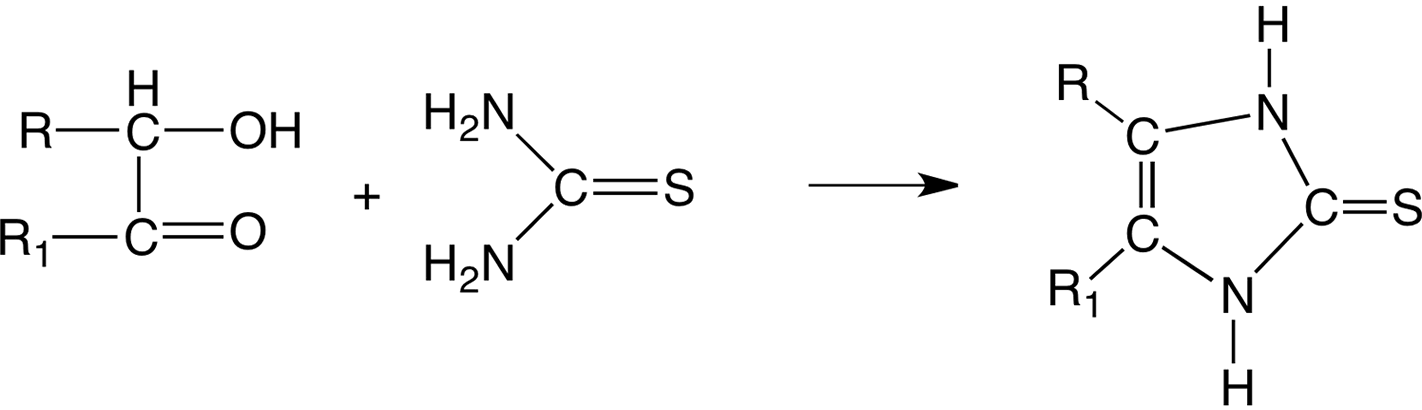
Con ácidos 2-oxocarboxílicos (por ejemplo, ácido pirúvico) se forma 2,3-dihidro-2-tioxo-4H-imidazol-4-ona:
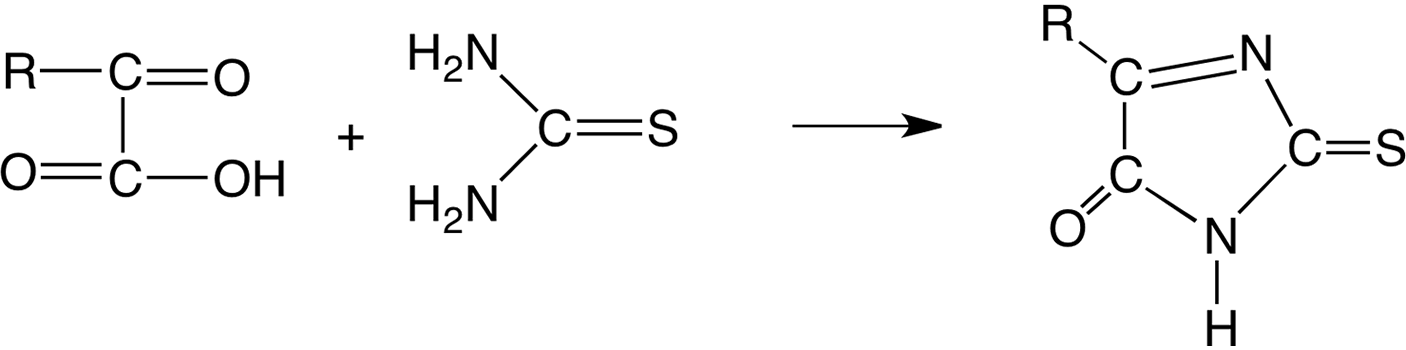
Ésteres malónicos reaccionan con la tiourea para dar ácido tiobarbitúrico:
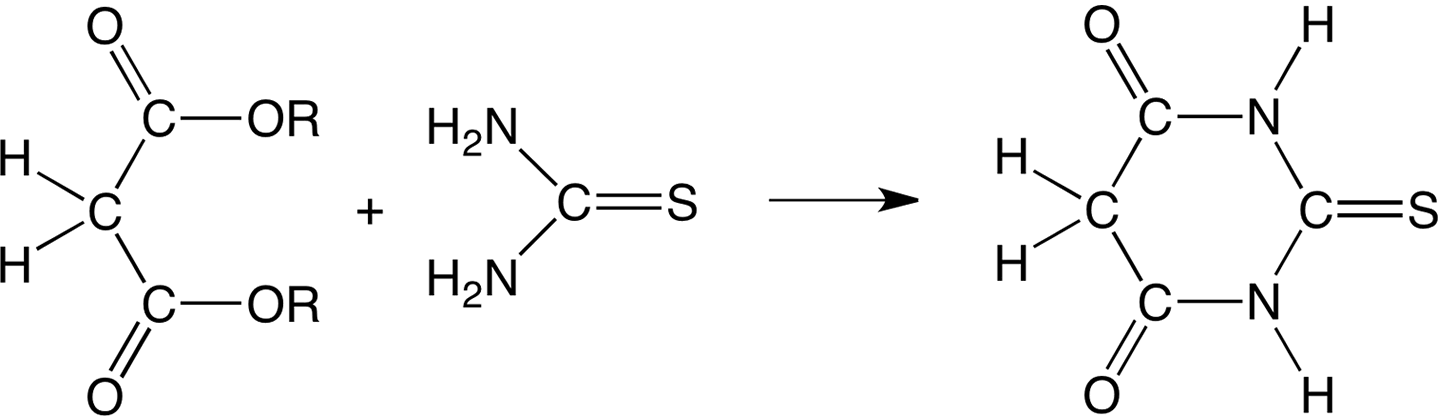
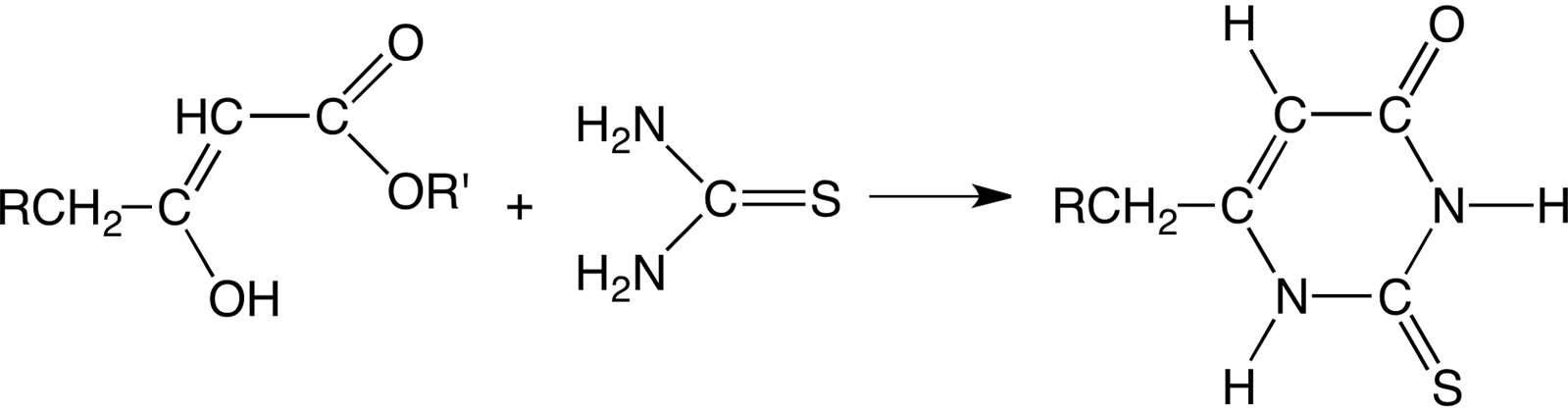
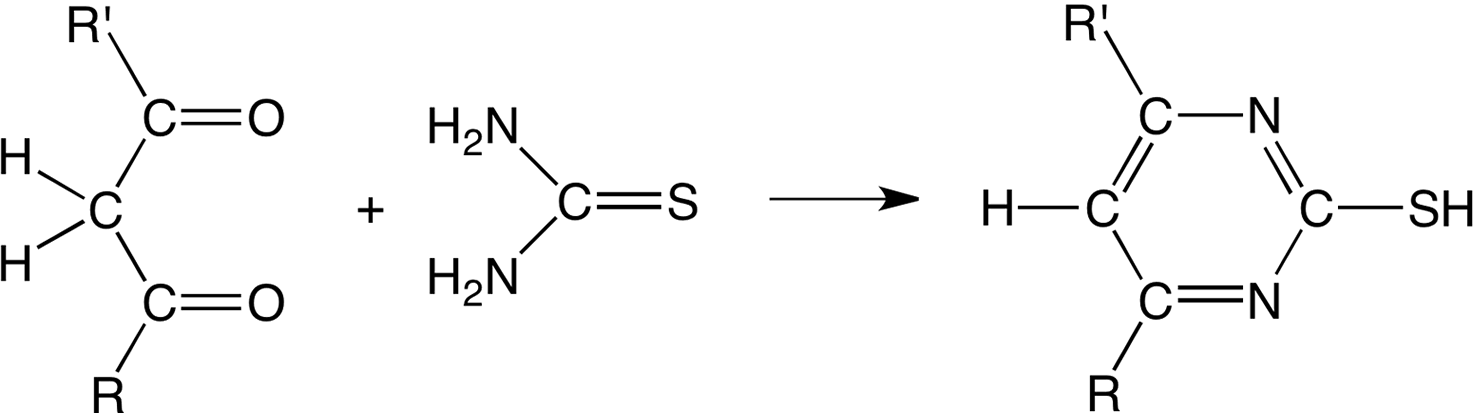
Ésteres de ácido 2-oxocarboxílico condensan con tiourea en tiouracilos, y con 1,3-dicetonas condensan a mercaptopirimidinas: