De la misma manera que para la entalpía, podemos plantear para la entropía:
Reactivos Productos ∆S = ¿?
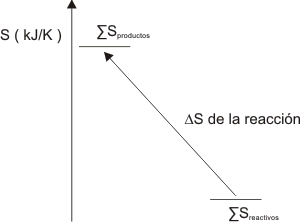
Gráfico número 24
Por supuesto si reactivos y productos están en sus estados normales tendremos ∆S°. Y hablando de estados normales retomemos el tema preguntándonos por qué la temperatura y la presión son importantes definirlas para tabular valores de entropía.
Temperatura: la energía cinética aumenta al hacerlo la temperatura lo cual debilita las fuerzas que unen a las moléculas dándoles mayor libertad de movimiento y por lo tanto desordenando el sistema. ¿Cómo será el efecto para moléculas que no tengan uniones intermoleculares muy apreciables?
Evidentemente bastante pequeño, lo cual se certifica observando que la entropía del oxígeno a 1 atm se eleva sólo el 4% cuando la temperatura se eleva de 25°C a 100°C. Recuerde que el oxígeno sólo tiene fuerzas de corto alcance que une las moléculas (Van der waals).
Presión: una disminución de presión aumenta la entropía ya que confina las moléculas en un mayor volumen y la inversa cuando aumenta la presión. Por supuesto este efecto es muy evidente en gases y poco en líquidos y sólidos. En un gas cuando se aumenta la presión de 1 a 10 atm decrece su S (entropía) en aproximadamente 19,22 J/K en un mol.
Veamos algunas entropías molares expresadas en J/K de sólidos, líquidos y gases:
Sólidos |
Líquidos |
Gases |
|---|---|---|
| C (diamante) 2,50 | H2O 69,80 | He 125,81 |
| Na 50,99 | Hg 77,33 | O2 205,23 |
| NaCl 72,31 | Br2 151,90 | Br2 244,94 |
¿Qué podemos deducir de esta tabla, que por supuesto es sumamente limitada?
En principio se manifiesta que los sólidos como grupo tienen entropías menores que los líquidos los que a su vez son menores que las de los gases. Es interesante el caso particular del bromo el cual en estado líquido tiene 152,15 J/K y en estado de gas 244,94 J/K. Como ve es significativa la diferencia entre ambos estados. Luego es importante saber el estado de agregación de la materia y por lo tanto cuando se tabulen valores de entropía hay que colocar el correspondiente sufijo “s”, “l” o “g”.
¿Qué ocurre en las reacciones químicas?
Casi invariablemente una reacción que se produce con aumento en el número de moles de gas se acompaña de un aumento de entropía y por supuesto si hay una disminución la misma será negativa. Esta regla es obvia en su deducción ya que al tener, por ejemplo, un mayor número de moles de gas estamos en presencia de un desorden aumentado.
En reacciones en las que no intervienen gases, frecuentemente se tiene que el aumento del número total de moles va acompañado de un aumento de entropía, especialmente cuando la diferencia en el número de moles es grande entre reactivos y productos.
Cambios de ∆S con la temperatura y la presión en reacciones químicas
El cambio de entropía en una reacción, por lo menos arriba de 25ºC es casi independiente de la temperatura.
¿Cómo podemos congeniar lo anterior con lo dicho de que para un compuesto individual su entropía aumenta con la temperatura? Es que en la mayoría de los casos el aumento de entropía de los productos casi iguala al de los reactivos y por lo tanto la diferencia de entropía (∆S) no cambia apreciablemente.
Al contrario de la temperatura, la presión influye considerablemente en el valor de ∆S, en especial cuando hay un cambio en el número de moles de gas.
A la luz de todos estos conocimientos usted ¿puede arriesgarse a postular si la entropía es una propiedad extensiva o intensiva?
Piense que para ser una propiedad intensiva no debe depender de la cantidad de masa del sistema. Por lo tanto la entropía es una propiedad extensiva.